在药品生产和销售领域,药品生产许可证是企业合法开展经营活动的必备证件。无论是新建药品生产企业还是已有的企业扩大生产范围,都必须按照相关法规要求,申请药品生产许可证。对于许多企业来说,药品生产许可证的申请流程可能显得复杂且繁琐。为了帮助企业更高效地完成申请工作,我们将通过简易流程图的形式,为您详细解读药品生产许可证的申请步骤。
在申请药品生产许可证之前,企业需要完成筹建工作,包括选址、厂房建设或租赁、设备购置以及人员招聘等。这一阶段的重点是确保企业的生产条件符合《药品生产质量管理规范》(GMP)的要求,这是药品生产许可证申请的核心标准之一。
资料准备是申请药品生产许可证的关键环节。根据国家药品监督管理局的规定,企业需要提交以下主要资料:
企业需要确保所有提交的资料真实、完整,并符合相关法规要求。
在资料准备完成后,企业可以通过线上或线下的方式向当地药品监督管理部门提交申请。线上申请通常通过国家药品监督管理局的官方网站进行,而线下申请则需要将纸质资料递交至当地药品监督管理局窗口。
药品监督管理部门在收到企业的申请资料后,会安排现场检查。检查的重点包括企业的生产环境、设备设施、质量管理体系以及人员资质等。企业需要提前做好迎接检查的准备工作,确保现场检查顺利通过。
现场检查通过后,药品监督管理部门会对企业的申请进行审核。审核通过后,企业将获得《药品生产许可证》。如果审核未通过,企业需要根据反馈意见进行整改,并重新提交申请。
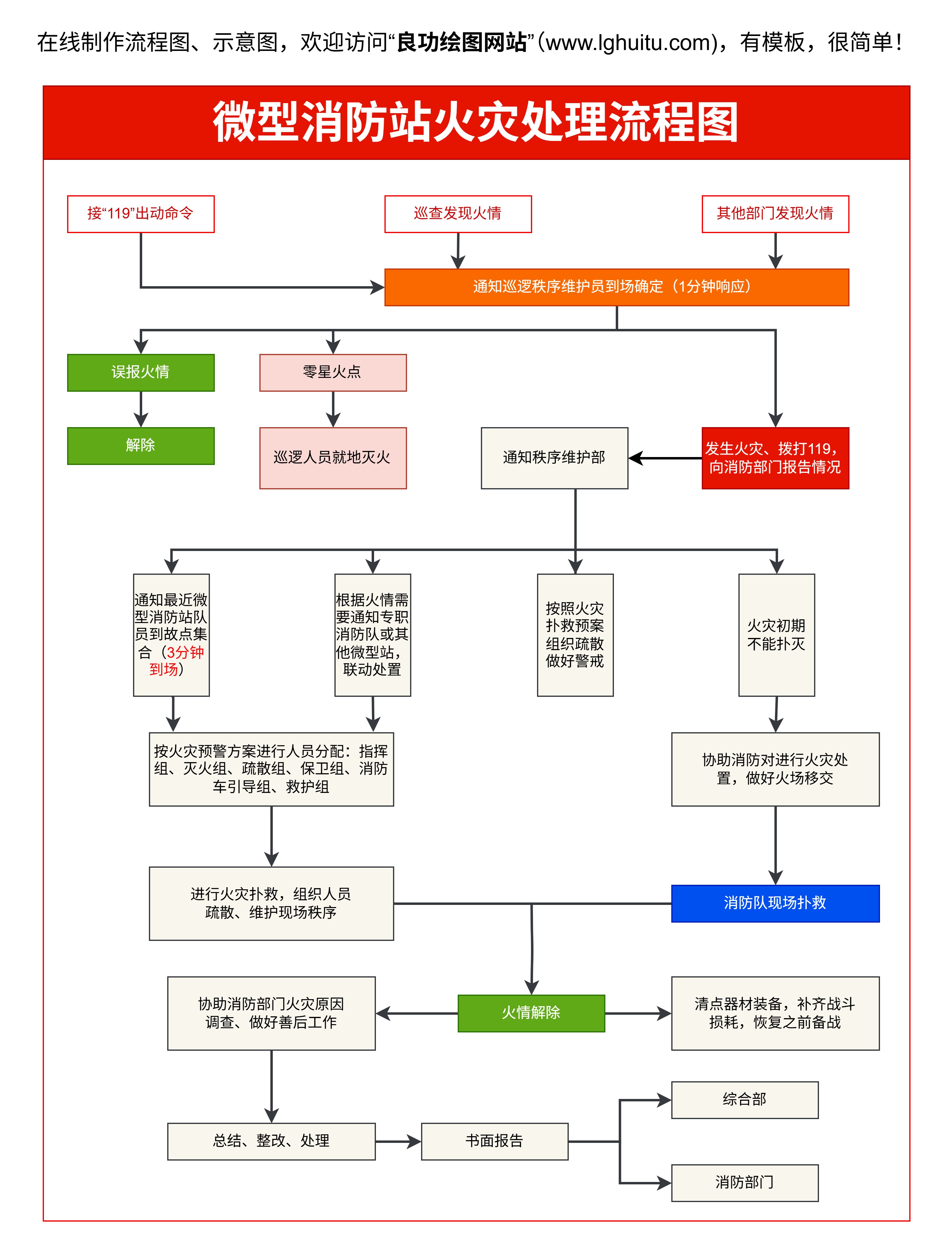
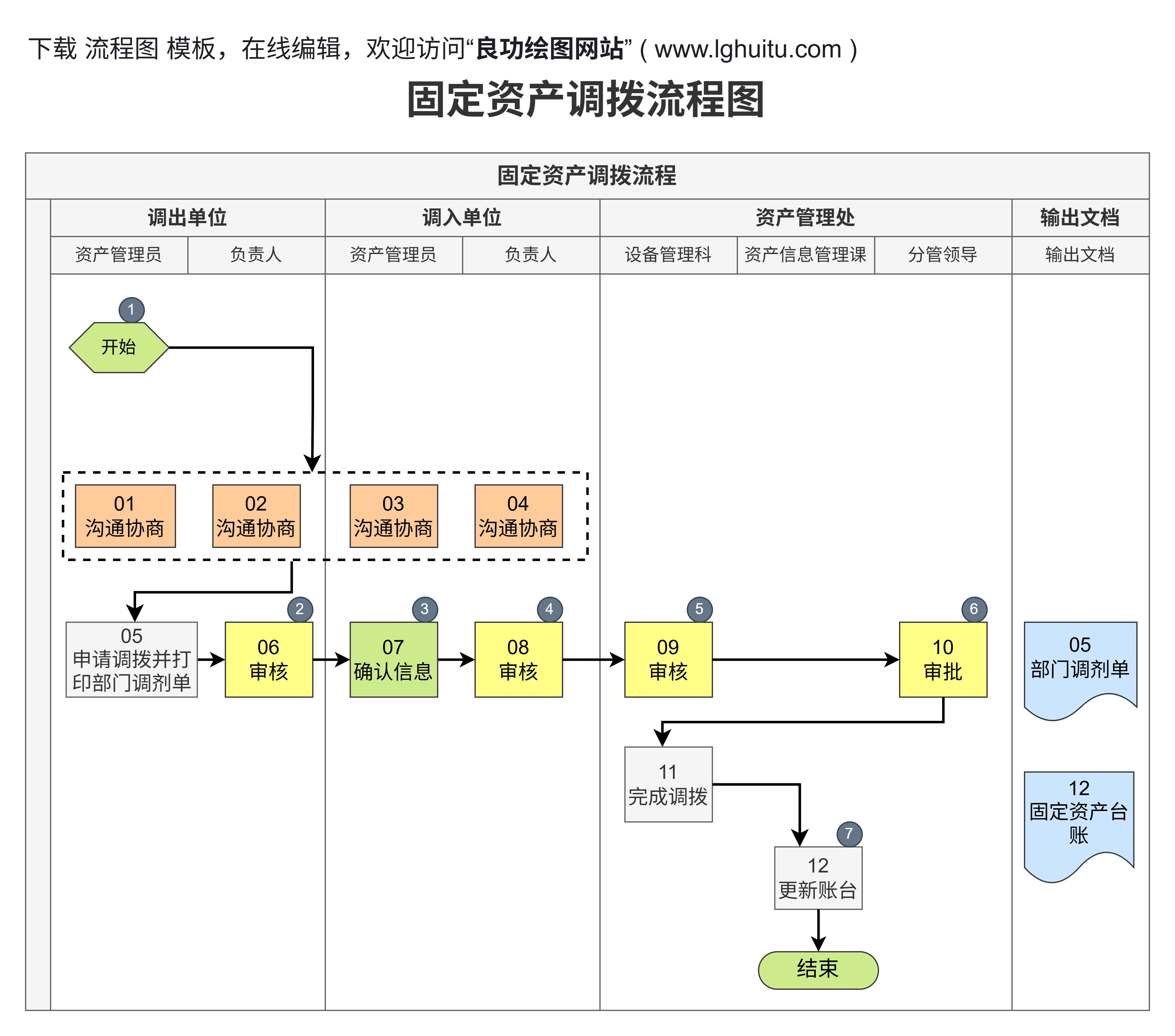
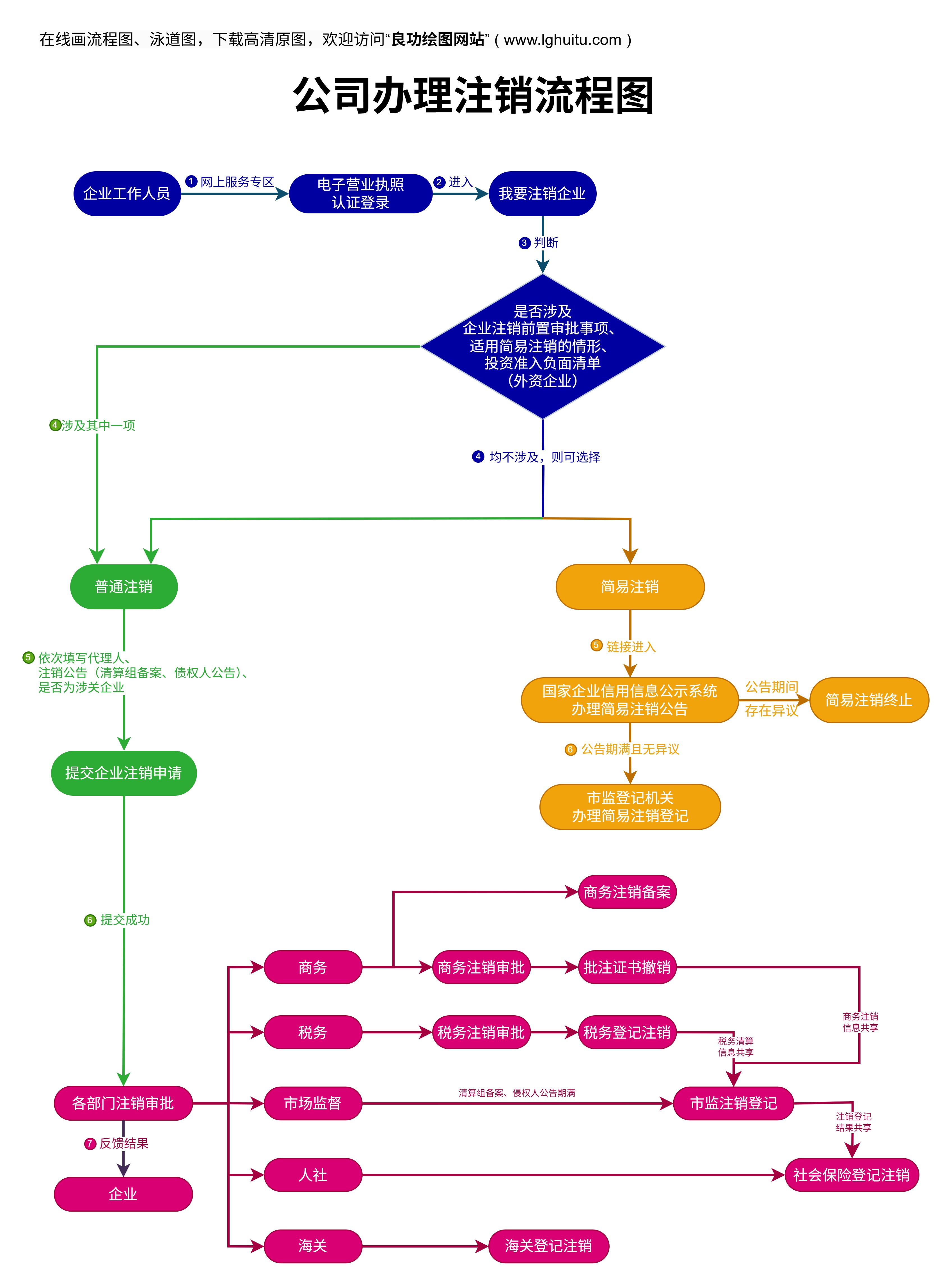
为了帮助企业更直观地理解药品生产许可证的申请流程,我们可以通过简易流程图的形式将整个过程可视化。以下是一个典型的药品生产许可证申请流程图示例:
通过这样的流程图,企业可以清晰地了解每个步骤的要求和时间节点,从而更高效地完成申请工作。
在药品生产许可证的申请过程中,企业需要注意一些关键点,以确保申请顺利通过并按时获得许可证。
《药品生产质量管理规范》(GMP)是药品生产许可证申请的核心要求之一。企业必须确保其生产过程符合GMP标准,包括厂房设施、设备管理、生产记录、质量控制等方面。如果企业的GMP体系不完善,可能会导致申请被退回或拒绝。
生产地址的选择直接影响到企业的生产条件是否符合法规要求。企业需要选择一个符合GMP标准的生产地址,并确保其周边环境不会对药品生产造成污染风险。生产地址的布局也需要合理,便于生产和质量管理。
企业的管理人员和技术人员必须具备相应的资质。例如,企业的法定代表人或负责人需要具备医药相关专业背景或管理经验,而质量管理人员则需要具备GMP认证资质。企业的生产技术人员也需要具备相应的专业技能和资质。
企业需要提前规划好药品生产许可证的申请工作,确保每个环节都有足够的时间完成。特别是在资料准备阶段,企业需要预留充足的时间来收集和整理相关文件,避免因资料不全或不规范而导致申请被退回。
对于首次申请药品生产许可证的企业,建议选择专业的咨询团队提供技术支持。专业的咨询团队可以帮助企业梳理申请流程、完善GMP体系、准备申请资料,并提供现场检查的模拟演练,从而提高申请的成功率。
药品生产许可证的申请流程和要求可能会随着法规的更新而发生变化。企业需要密切关注国家药品监督管理局的相关政策动态,确保申请工作符合最新的法规要求。
获得药品生产许可证后,企业仍需持续关注许可证的有效期和年检要求。根据相关规定,药品生产许可证的有效期为5年,企业需要在有效期届满前重新申请换证。企业还需要定期接受药品监督管理部门的监督检查,确保生产条件和质量管理持续符合要求。
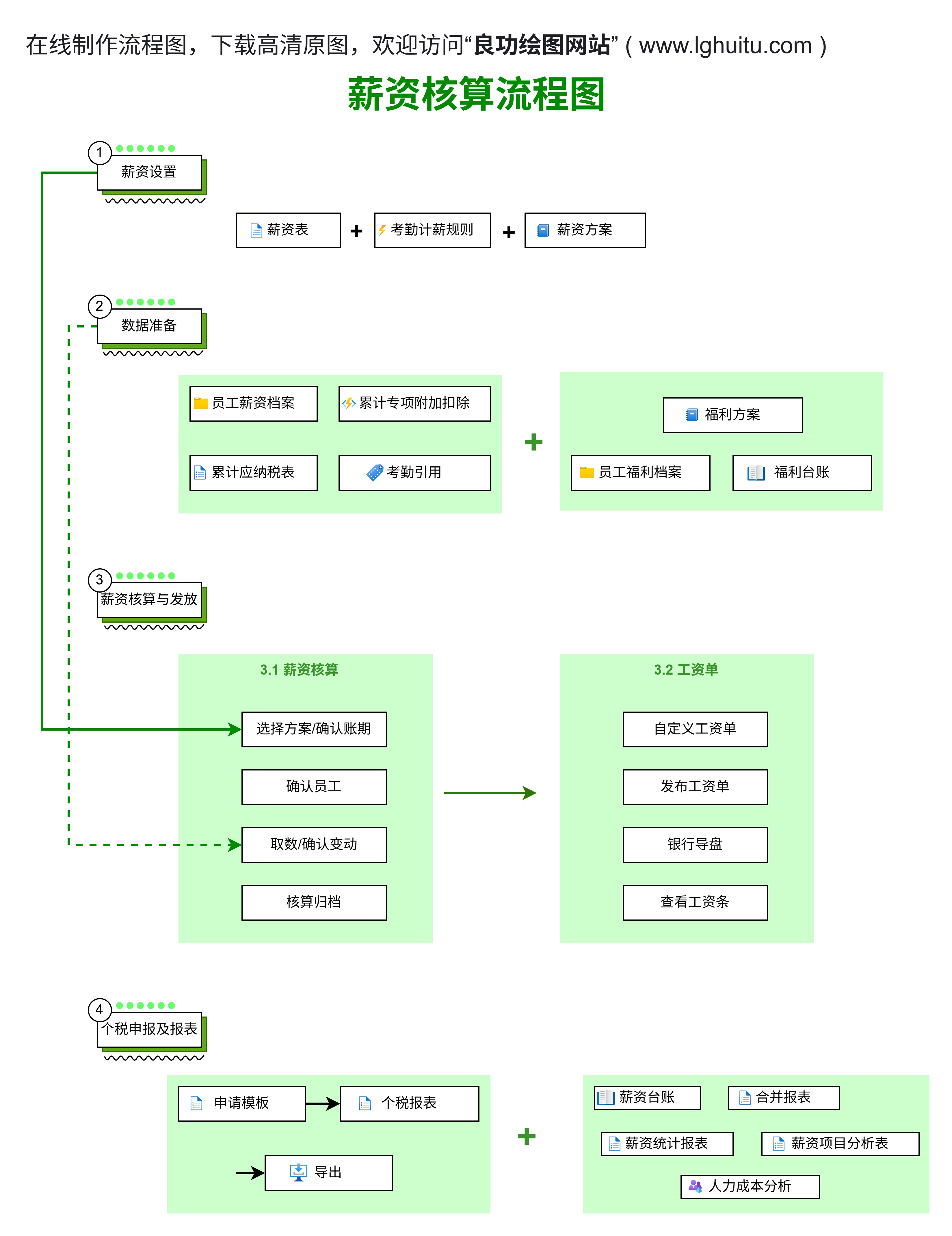
通过简易流程图的形式,企业可以更直观地掌握药品生产许可证的申请流程,并根据流程图进行操作。以下是一个药品生产许可证简易流程图的实际应用示例:
通过这样的流程图,企业可以清晰地了解每个步骤的要求和时间节点,从而更高效地完成申请工作。
药品生产许可证的申请流程虽然复杂,但通过提前规划和准备,企业可以更高效地完成申请工作。简易流程图的形式可以帮助企业更直观地掌握申请步骤,确保每个环节都符合法规要求。企业也需要关注法规变化,持续完善生产条件和质量管理,确保许可证的有效性和合规性。希望本文能够为您的药品生产许可证申请工作提供有价值的参考和指导!